Tecnologia Científica
Transferência inesperada de elétrons do hidrogênio para metais reformula a compreensão de reações químicas essenciais
Acelerar reações químicas é fundamental para aprimorar processos industriais ou mitigar resíduos indesejados ou nocivos. Para concretizar essas melhorias, os químicos devem projetar com base em vias de reação documentadas.
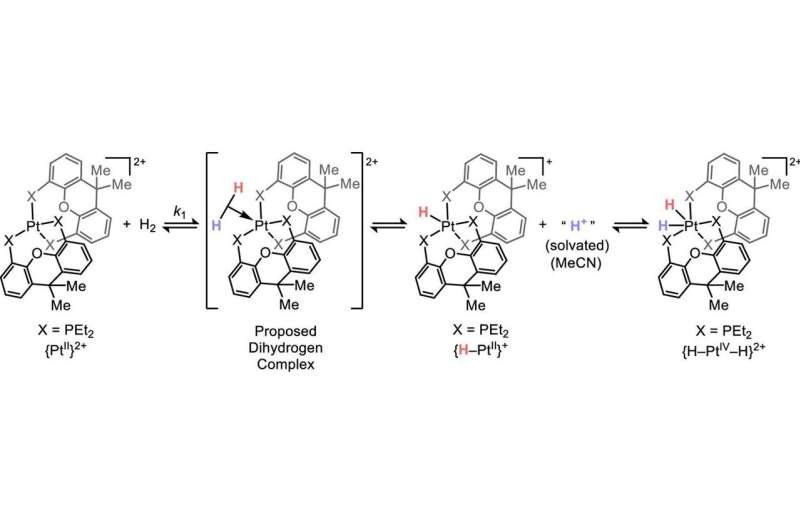
Novas pesquisas mostram que a adição oxidativa líquida pode ocorrer por meio de uma ordem diferente de eventos, na qual o complexo de metal de transição aceita elétrons de um substrato orgânico (H2). Crédito: Universidade Estadual da Pensilvânia
Acelerar reações químicas é fundamental para aprimorar processos industriais ou mitigar resíduos indesejados ou nocivos. Para concretizar essas melhorias, os químicos devem projetar com base em vias de reação documentadas. Agora, uma equipe de pesquisadores da Penn State descobriu que uma reação fundamental chamada adição oxidativa pode seguir um caminho diferente para atingir os mesmos objetivos, levantando a questão de se essa nova ordem de eventos já vinha ocorrendo desde o início e potencialmente abrindo novas possibilidades para o design químico.
Um artigo descrevendo a pesquisa aparece no Journal of the American Chemical Society .
As reações de compostos orgânicos — aqueles que contêm carbono, hidrogênio, oxigênio e alguns outros elementos — são limitadas pelos padrões de ligação e arranjos eletrônicos específicos dos elementos orgânicos. Mais arranjos eletrônicos estão disponíveis em metais de transição, outro tipo de elemento que inclui, por exemplo, platina e paládio.
Quando metais de transição interagem com compostos orgânicos, essa camada adicional de complexidade pode modificar a estrutura eletrônica dos compostos orgânicos, levando a uma maior diversidade de reações potenciais, incluindo a quebra de ligações químicas e a catalisação de reações impossíveis entre compostos puramente orgânicos . Compreender a diversidade de maneiras pelas quais essas reações químicas podem ocorrer pode ajudar os químicos a desenvolver maneiras de explorar metais de transição para aumentar a eficiência de processos industriais ou encontrar novas soluções que possam, por exemplo, ajudar a reduzir os poluentes ambientais, de acordo com os pesquisadores.
"Os metais de transição têm propriedades que lhes permitem 'quebrar as regras' da química orgânica ", disse Jonathan Kuo, professor assistente de química no Eberly College of Science da Penn State e líder da equipe de pesquisa. "Por exemplo, embora os sistemas biológicos sejam amplamente considerados orgânicos, grande parte da química nas células ocorre em sítios ativos, onde cofatores metálicos, na verdade, determinam a reatividade."
Metais de transição também são usados para catalisar reações químicas em escala industrial. Compreender como essas reações funcionam é uma maneira de se aproximar da eficiência da natureza ou até mesmo inventar reações que não tenham analogia conhecida na natureza.
As reações químicas ocorrem porque os átomos que compõem as moléculas "querem" estar em um estado mais estável. Essa estabilização é realizada principalmente pelo rearranjo dos elétrons entre os orbitais — as regiões semelhantes a nuvens ao redor dos núcleos atômicos, onde os elétrons provavelmente estão localizados. Um átomo de hidrogênio, por exemplo, possui apenas um elétron que reside em um orbital "1s".
No entanto, dois átomos de hidrogênio podem se ligar para formar di-hidrogênio (H2), onde os dois orbitais 1s se misturam para formar dois orbitais híbridos. O mais estável dos dois orbitais híbridos hospeda os dois elétrons, resultando em economia líquida de energia e maior estabilidade. Elementos maiores e mais complexos podem ter múltiplos orbitais s com diferentes níveis de energia, bem como orbitais p, d e f, que possuem formas e capacidades variadas, levando a uma maior diversidade na estrutura eletrônica e a mais tipos possíveis de reações químicas.
"Na natureza, um átomo de hidrogênio só consegue sustentar seu elétron usando seu único recurso orbital, o orbital 1s", disse Kuo. "Mas dois átomos de hidrogênio podem se unir e dizer: 'Temos dois elétrons e dois recursos orbitais; qual é a maneira mais eficiente de compartilhar a carga entre nossos recursos?' A maioria dos elementos orgânicos possui apenas orbitais s e p, mas os metais de transição adicionam orbitais d à mistura."
Na maioria das descrições de adição oxidativa, diz-se que os metais de transição doam seus elétrons para substratos orgânicos durante o processo de ligação. A proximidade da molécula orgânica ao metal de transição permite que os dois conjuntos de orbitais se misturem, desencadeando diversos tipos de reações. Por esse motivo, tem havido muito esforço para desenvolver compostos de metais de transição com densidade eletrônica, o que potencialmente os tornaria ativadores mais potentes.
"No entanto, observou-se que algumas adições oxidativas são um pouco diferentes", disse Kuo. "Um subgrupo é, na verdade, acelerado por compostos de metais de transição deficientes em elétrons. Conseguimos identificar uma explicação plausível, onde, em vez de o metal de transição doar elétrons, a primeira etapa da reação envolveu elétrons se movendo de uma molécula orgânica para o metal de transição. Esse tipo de fluxo de elétrons, conhecido como heterólise, é bem conhecido, mas não havia sido observado anteriormente que resultasse em uma adição oxidativa líquida."
A equipe de pesquisa utilizou compostos contendo os metais de transição platina e paládio — que não eram eletrodensos — e os expôs ao gás hidrogênio. Em seguida, utilizaram espectroscopia de ressonância magnética nuclear para monitorar as alterações no complexo do metal de transição. Dessa forma, puderam observar uma etapa intermediária, indicando que o hidrogênio havia doado seus elétrons ao complexo metálico, antes de se aproximar de um estado final resultante indistinguível da adição oxidativa.
"Estamos entusiasmados em adicionar esta nova estratégia ao manual dos metais de transição", disse Kuo. "Mostrar que isso pode ocorrer abre novas e empolgantes maneiras de usar a química dos metais de transição. Estou especialmente interessado em encontrar reações que possam decompor poluentes persistentes."
Além de Kuo, a equipe de pesquisa inclui a primeira autora Nisha Rao, uma estudante de pós-graduação em química na Penn State.
Mais informações: Nisha Rao et al., Adição oxidativa líquida de H? a {MII}? (M = Pd, Pt) por heterólise e rebote prótico, Journal of the American Chemical Society (2025). DOI: 10.1021/jacs.5c07140
Informações do periódico: Journal of the American Chemical Society